はじめに
リアルワールドデータ(以下、RWD)を用いた薬剤疫学研究は、ランダム化比較試験(RCT)では捉えきれない、実臨床における薬剤の使用実態や有効性、安全性の評価を行ううえで不可欠な手法となっています。
しかし、RWDは臨床研究のために設計されたものではないため、カルテや処方記録から把握できるのは「処方した」という事実までで、患者さんが「実際にどう服薬したか」を正確に知ることは困難です。
そのため、データベース(以下、DB)研究をすすめるうえで、この「実際の服薬や臨床的判断と、データ上の処方のズレ」という課題に直面します。このズレをどのように扱うかが、研究結果の信頼性を大きく左右します。
本稿では、この「ズレ」を乗り越え、より実態に近い「治療継続」を定義する方法について、
- ケース①:受診遅れ
- ケース②:薬剤の重複処方
という臨床現場でよく起こる2つのケースにおける代表的な考え方を解説します。
ケース①:受診遅れへの対処
受診遅れが引き起こすRWDでの処方と実際の服薬のズレ
高血圧で定期通院中のAさんがいるとします。いつもは28日分の薬剤がなくなる頃に来院しますが、今回は仕事の都合で受診が遅れたため、前回の処方から30日目(2日遅れ)に来院しました。こういったケースにおいて、臨床的には、「治療は継続している」と判断します。
一方、RWDでは以下の様にデータが格納されています。
- 2025年8月1日 高血圧薬A 処方日数:28日
- 2025年8月31日 高血圧薬A 処方日数:28日
もし、単純に「処方日数の終わりまでに次の処方がなされていない場合を薬剤の中止」と定義すると、DB研究上ではAさんは8月29日の時点で薬剤を中止していることになってしまいます。
しかし、高血圧に対する数年間の治療において2日間の内服中断は薬剤を継続していると臨床的には判断できます。
このような経緯で、「臨床的判断とRWDでの処方のズレ」が生まれます。
Grace period(猶予期間)とは?
このような処方と次の処方の間を補正するために用いられる概念が「Grace period」です。Grace periodとは「処方期間終了後に、医薬品の飲み残しや中止した医薬品の効果が持続することを考慮し、追加される期間」のことです。
言い換えると、処方と次の処方の間隔について、どの程度のバッファを持った日数までを継続とみなすかという閾値です。処方と次の処方の間隔がGrace periodよりも短ければ治療継続、超えた場合はGrace periodの最終日を治療中止日とします。
例として、研究者が設定したGrace period を基に、治療継続期間を求める過程を示します(図1)。
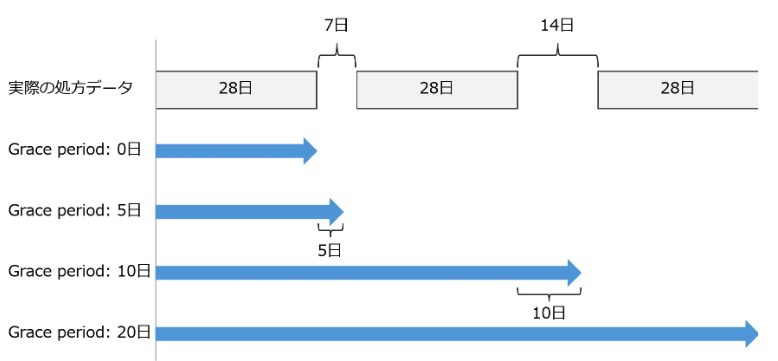
処方データとして、患者さんは28日毎に処方を受けず、7日間や14日間の処方を受けていないギャップの期間があるとします。
ここで、 Grace period を0日、10日、20日と設定した場合の、それぞれの治療継続期間を見てみましょう。
Grace period が0日では、28日の処方分が終了した時点で治療中止となります。よって、この場合の治療継続期間は28日間です。
Grace period が10日では、28日の処方分が終了した後7日間のギャップを超えて治療継続となります。再度28日の処方分が終了した後10日間は治療継続とします。しかし、そこまでの時点で追加処方がないため治療中止となります。よって、この場合の治療継続期間は73日間です。
Grace period が20日では、7日間の1回目のギャップと14日間の2回目のギャップを超えて治療継続とします。よって、この場合の治療を中止せず継続しているとみなされます。
Grace periodを研究ではどのように設定するのか?
現状では、Grace periodを何日と決めるためのゴールドスタンダードはありません。
手持ちのデータにおける処方日数の分布、薬剤の半減期、および専門家の意見を参考に薬剤終了後に効果が持続すると想定される期間を考慮に入れて妥当な期間を設定します。2型糖尿病治療薬に関する研究では、Grace periodが30日・90日・180日など30日の倍数で設定されていました4。
ケース②:薬剤の重複処方
残薬が引き起こすRWDでの処方と実際の服薬のズレ
臨床では、「連休に入る前に」「仕事の都合で」といった理由で、患者さんが手元の薬を使い切る前に来院し、次の処方を受けることも頻繁にあります。この場合、臨床では、手元に薬が少し余る(ストックされる)ため、その分を含めて服薬は継続されると判断します。
一方、RWDでは以下の様にデータが格納されています。
- 2025年8月1日 高血圧薬B 処方日数:30日
- 2025年8月26日 高血圧薬B 処方日数:30日
DB研究を実施する際に、5日間の重複を無視して単純に処方期間を計算すると(25日間+30日間=55日間)、患者さんが実際に薬を手にしていた期間(30日+30日=60日分)よりも過小評価につながります。このような経緯で、「実際の服薬とRWDでの処方のズレ」が生まれます。
この「処方期間の重複による薬剤の蓄積」をStock-pilingと呼びます。
Stock-pilingの対処方法は?
この問題を解決するため、DB研究では「重複した処方日数を、次の処方期間に加算する」という繰り越し(キャリーオーバー)方式がよく用いられます。
先ほどの例では、DB研究を実施する際に、重複となる5日間を無視せずに、医薬品の曝露期間とします。つまり、重複した5日分を次の処方期間に加算することで、治療継続期間は60日間と計算され、より実態に近い評価が可能になります。
Stock-pilingの対処方法で残る問題点
ただし、この方法にも注意点があります。毎回早めに受診する患者さんの場合、繰り越し分が雪だるま式に増え続け、計算上は手元に数ヶ月分のストックがあることになりかねません。これは、実際の服薬状況を過大評価するリスクがあります。
そのため、DB研究では「繰り越しの上限を設ける(例:最大90日まで)」といったルールを追加し、臨床的な妥当性を担保することがあります5。
さいごに
DB研究は、私たちの日常診療から得られる貴重なエビデンスの源泉です。しかし、そのデータが「処方記録」であり、「完全な服薬記録」ではないという限界を理解しておく必要があります。
今回ご紹介しきれませんでしたが、 薬剤の曝露定義には、薬剤の追加(Add-on)や変更(Switching)をどう扱うかという論点もあります。さらに、注射薬や吸入薬、外用薬など、剤形によっても考慮すべき点は異なります。
弊社では、評価したい医薬品ごとに臨床での使われ方を理解した上で、「DB上の医薬品定義」を支援しています。お困りの際は、ぜひ一度ご相談ください(ご相談・お問い合わせはこちら)。
参考文献
1. 独立行政法人 医薬品医療機器総合機構. 医療情報のデータベース等を用いた医薬品の安全性評価における薬剤疫学研究の実施に関するガイドライン 初版. 2014.
2. 佐藤 俊哉, 山口 拓洋, 石黒 智恵子. これからの薬剤疫学 ーリアルワールドデータからエビデンスを創るー. 朝倉書店. 2021.
3. 深澤 俊貴, 岩上 将夫, 原 梓, 漆原 尚巳. 企画/リアルワールドエビデンス研究の再現性向上に向けた調和プロトコルテンプレート(HARPER) デザインダイアグラム:リアルワールドデータを活用した研究デザインを可視化し,再現性を高めるフレームワーク. 薬剤疫学. 2023;28(2):39-55.
4. Weisman A, King LK, Mamdani M. Reporting and variability of constructing medication treatment episodes in pharmacoepidemiology studies: A methodologic systematic review using the case study of DPP-4 inhibitors and cardiovascular outcomes. Pharmacoepidemiol Drug Saf. 2020 Aug;29(8):939-950.
5. Fisher A, Carney G, Bassett K, Dormuth CR. Tolerability of Cholinesterase Inhibitors: A Population-Based Study of Persistence, Adherence, and Switching. Drugs Aging. 2017 Mar;34(3):221-231.